本文回顾性分析我院4例Zinner综合征患者的临床资料并结合相关文献复习,对Zinner综合征的诊断、治疗等进行讨论。其中1例行腹腔镜下精囊囊肿及输尿管切除术,1例经直肠精囊囊肿穿刺抽吸术,2例保守治疗。行腹腔镜切除术者出院后随访未见并发症及复发征象。行经直肠精囊囊肿穿刺抽吸术者出院1个月后随访,患者症状消失,但经盆腔CT提示精囊囊肿大小同术前,考虑复发。保守治疗者未见明显不适。
In this article, we retrospectively analyzed the clinical data of four patients with Zinner syndrome at our institution and discussed the diagnosis, treatment and other aspects of Zinner syndrome in conjunction with a review of relevant literature.One patient underwent laparoscopic seminal vesicle and ureterectomy, 1 patient underwent transrectal seminal vesicle aspiration and 2 were treated conservatively.None had complications or signs of recurrence after laparoscopic resection.After 1 month of hospital discharge, patients were followed up for transrectal aspiration of seminal vesicles, and the symptoms disappeared, but pelvic CT suggested that the seminal vesicles were the same size as before operation and recurrence should be considered.No significant discomfort was seen with conservative treatment.
Zinner综合征由Zinner1914年最先报道, 是一种罕见的先天性男性泌尿生殖系统病变, 常表现为精囊囊肿(seminal vesiclecyst, SVC)、同侧肾发育不全或肾缺如及同侧射精管梗阻三联征[1]。其也被认为是女性苗勒管发育不全(Mayer-Rokitansky-Kuster-Hauser, MRKH)综合征对应的男性病症[2]。该病患者通常体检偶然发现或出现临床症状时被发现, 治疗常由患者症状严重程度所决定。本文报道了我院近3年收治的4例Zinner综合征患者。
患者平均年龄 28.5岁。2例因出现临床症状确诊Zinner综合征, 其中例1表现为下腹部疼痛, 左侧阴囊肿痛伴尿痛; 例2主要为肛门区坠胀感。另外2例因体检偶然发现。4例患者均能通过直肠指检触及质软肿物, 例1因合并左侧附睾炎, 左侧阴囊皮肤潮红, 睾丸触压痛明显。所有患者均行CT泌尿系造影(CTU)(图1), 均符合一侧精囊囊肿, 同侧肾发育不全及同侧射精管梗阻三联征表现。其中, 例1因阴囊肿痛行阴囊彩超提示合并左附睾炎, 例2则出现双侧精囊囊肿的罕见影像学表现(图1 D)。
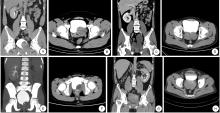 | 图1 术前CT泌尿系造影 A:例1冠状面图像显示左肾缺如; B:横断面图像显示左侧精囊囊肿; C:例2冠状面图像显示左肾缺如及左侧输尿管扩张; D:横断面图像显示双侧精囊囊肿; E:例3冠状面图像显示左肾缺如; F:横断面图像显示左侧精囊囊肿; G:例4冠状面图像显示右肾缺如; H:横断面图像显示右侧精囊囊肿 |
2例手术治疗, 2例保守治疗。其中, 例1选择全麻下行腹腔镜下左侧精囊囊肿切除术+左侧输尿管切除术+膀胱镜检查术。膀胱镜见膀胱左后壁半圆形粘膜下肿物突入膀胱, 未见左侧输尿管口, 右侧输尿管口位置正常。经腹途径腹腔镜打开左腹膜后间隙, 找到左侧扩张输尿管残端, 近端为盲端, 向输尿管远端游离, 可见膀胱左后方精囊区一明显膨大的肿物, 考虑左侧残余输尿管异位开口于左侧精囊囊肿, 小心游离至前列腺底部平面, 完整切除囊肿及左侧输尿管, 处理创面, 留置左侧盆腔引流管1根, 结束手术。术后第4天出院, 术后病理符合精囊囊肿。例2截石位局部麻醉下经直肠B超引导使用18 G穿刺针行双侧精囊囊肿穿刺抽吸术, 抽出混浊囊液, 送液基细胞学病理。术后病理提示精囊液未见肿瘤细胞, 涂片见较多精子及大量退变的细胞。例3-4因无临床症状, 选择定期超声复查, 待囊肿明显增大或出现临床症状再考虑手术治疗。所有患者随访4~12个月, 例1出院1个月后复查膀胱CT:左侧精囊腺囊肿、左侧输尿管囊肿未见复发。例2出院后1月盆腔CT提示左侧精囊囊肿复发, 大小约69 mmx23 mm。2例保守治疗患者无明显不适症状, 继续定期复查。
Zinner综合征极其罕见, 台湾有研究人员通过对280000例儿童进行筛查, 发现Zinner综合征的发生率为0.0046%(13/28000)[3]。正常情况下, 从胚胎发育第5周开始, 在雄性激素及抗苗勒管激素的影响下, 中肾管末端可发育为输精管、附睾、射精管、膀胱颈等结构, 且其末端还可发出输尿管芽, 输尿管芽与后肾芽基相互作用, 继续分化形成输尿管和肾集合系统等结构。当中肾管发育出现异常时, 常可同时出现肾脏缺如或发育不全及生殖系统异常的情况[4]。其临床症状与精囊囊肿大小、感染、出血明显相关, 直径< 5cm的囊肿通常无症状; 当精囊囊肿≥ 5cm时, 常见症状是腹部、盆腔或会阴部反复疼痛; 还会出现与压迫相关的非特异性临床症状; 另外, 附睾炎或慢性前列腺炎也有报道[5]。
本文报道的例1患者合并附睾炎, 考虑由于射精管阻塞形成精囊囊肿并感染, 再沿输精管道逆行感染引起的附睾炎; 或由于精液排出不畅导致附睾精液聚集引起。例2患者因精囊囊肿压迫直肠导致肛门区坠胀不适; 检查发现双侧精囊囊肿, 先天性左肾缺如; 像这样一侧肾缺如合并双侧精囊囊肿的病例十分少见, van den Ouden等[6]报道Zinner综合征中合并双侧SVC仅2%。另外2例暂无临床症状, 充分说明该病症状隐匿且多样。有研究报道Zinner综合征左右侧发病率相同[7]。本文报道的4例患者左右发病率比值为3:1, 考虑为例数相对较小导致的偏差。
Zinner综合征的诊断, 盆腔超声是首选检查[8], 但还需要进一步的辅助检查明确诊断, 包括经直肠超声检查、静脉尿路造影、CT扫描、磁共振成像以及膀胱镜检查。经直肠超声检查可以明确肿物的大小、位置及性质, 准确性高于盆腔超声, 但其视野较小[9]。静脉尿路造影可以评估肾及输尿管的异常, 以及囊肿是否与尿路相通[10]。CT扫描优于超声检查, 能准确显示盆腔解剖结构, 并能明确是否合并肾发育不良或肾缺如; 然而, CT对精囊囊肿与相邻结构是否相通较难判断。MRI被认为是诊断Zinner综合征的金标准, 因为它对软组织有更高分辨率, 盆腔解剖结构更加清晰, 准确性明显优于CT[9]。膀胱镜检查可以更直观地了解囊肿与尿路的关系, 了解输尿管及射精管开口情况, 同时可根据情况经尿路进行相关的治疗[11]。
Zinner综合征的治疗方面, 对于无症状者, 保守治疗是普遍接受的, 并需要长期随访。当囊肿较大或有症状患者应积极采取手术治疗, 手术方式包括经直肠或经会阴精囊囊肿抽吸术、经尿道精囊囊肿去顶术、开放手术、腹腔镜或机器人精囊囊肿切除术等[12]。单纯囊肿穿刺抽吸术可分为经直肠或经会阴途径, 复发率高, 且感染风险较高, 特别是经直肠囊肿的穿刺[6]。本文病例2经直肠囊肿穿刺术后1个月复查盆腔超声提示精囊囊肿复发, 虽然短期症状明显改善, 但是远期复发率较高, 不推荐作为首选方法。对于射精管远端梗阻患者, 可行经尿道射精管切开术, 操作简单, 效果显著, 且经自然通道更符合生理结构, 但可能术后有逆行射精的风险[13]。对于传统开放手术, 由于精囊位于膀胱后方, 位置较深, 传统开放手术不仅手术创伤大, 操作难度高, 还可能导致严重并发症, 包括膀胱、输尿管、直肠、对勃起功能起重要作用的血管神经束损伤等[12]。因此开放手术逐渐被腹腔镜精囊囊肿切除术替代。1995年, Carmingnani等[14]完成第一例腹腔镜下精囊囊肿切除术。腹腔镜手术与开放手术相比具有创伤小, 膀胱及直肠损伤的风险较小, 具有良好手术视野以及恢复快等优势。本文例1患者采用腹腔镜下左侧精囊及输尿管切除术, 术中损伤小, 术后恢复快且无明显并发症。
然而, 我们的样本量较少, 需要更多的病例数来验证腹腔镜手术治疗Zinner综合征的安全性及有效性。近年随着机器人技术的成熟, 机器人辅助腹腔镜下精囊囊肿切除术被认为是最佳手术方式[15]。综上, 4例患者提示一侧肾缺如或发育不全合并同侧盆腔内占位, 需考虑Zinner综合征可能。精囊囊肿较大或有明显症状患者可采取腹腔镜手术或机器人辅助腹腔镜囊肿切除术, 具有损伤小、并发症少、恢复快等特点, 是一种比较安全有效的治疗方式。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|


