良性前列腺增生(benign prostatic hyperplasia, BPH)是由于解剖学上的前列腺增大(benign prostatic enlargement, BPE), 引起尿动力学上以膀胱出口梗阻(bladder outlet obstruction, BOO)和以下尿路症状(lower urinary tract symptoms, LUTS)为主的临床症状[1]。对于中、重度症状BPH的患者, 外科干预是有效的治疗方案。外科手术的选择中, 经尿道前列腺电切除术(transurethral resection of prostate, TURP)仍是金标准, 近年来钬激光前列腺剜除术(holmium laser enucleation of prostate, HoLEP)或前列腺选择性汽化消融术(photoselective vaporization, PVP)得到了广泛应用, 效果与TURP相当[2], 随着科技的发展, 越来越多的微创技术被应用于BPH的治疗[3], 其中机器人水刀前列腺消融术以其快速、有效、无热损伤等特点受到关注[4]。2020年1月, 中国人民解放军总医院第一医学中心率先在国内完成2例机器人水刀前列腺消融术, 现将其早期经验报告如下。
2020年1月, 2名男性患者于中国人民解放军总医院第一医学中心接受机器人水刀前列腺消融术。例1, 67岁, 前列腺体积51.4 mL, 前列腺国际前列腺症状评分(international prostate symptom score, IPSS)27分, 生活质量评分 (quality of life, QOL)5分, 最大尿流率(max flow rate, Qmax)6.1 mL/s, 术前总前列腺特异性抗原(total prostate specific antigen, tPSA)0.965 μ g/L。例2, 69岁, 前列腺体积53.6 mL, IPSS评分20分, QOL评分4分, Qmax 3.2 mL/s, 术前总PSA 4.27 μ g/L。患者及家属术前均知情并签署知情同意书。纳入标准:确诊为BPH, 以LUTS为主要临床症状, 药物治疗无效, 临床评估符合手术指征的患者; 影像学提示前列腺体积增大; Qmax< 10 mL/s; 尿流动力学提示存在膀胱颈口梗阻、逼尿肌收缩良好; IPSS≥ 12分。排除标准:诊断为前列腺癌的患者; 既往有前列腺手术史; 有心肺功能不全等严重手术禁忌证等。
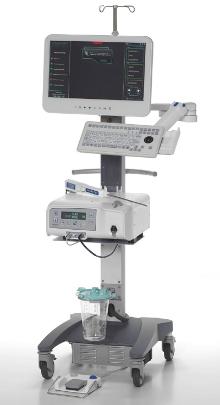
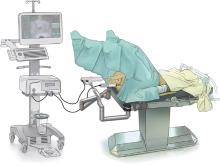
1.2.1 设备连接和放置 机器人水刀前列腺消融术使用的设备是AquaBeam系统(PROPECT BioRobotics® ), 由三个主要部件组成:共型规划单元、控制台、机器人手件(图1, 图片授权于PROPECT BioRobotics® )。2例患者均采用喉罩全麻。首先, 将经直肠探头置入直肠, 将超声视野调整为矢状位, 能观察到整个前列腺及部分膀胱, 并固定在一条床旁机械臂的步进器上。将定制的硬性膀胱镜安装在手件中的镜鞘内, 连接光源和成像设备, 将镜鞘用步进器推至手件顶端, 于直视下进入膀胱, 使膀胱镜远端与膀胱颈平齐, 观察前列腺的镜下形态, 向膀胱内突起的程度、膀胱颈形态、输尿管口的开口位置。将手件的机械端与动力盒连接并固定在另一条床旁机械臂上, 体位及设备摆放位置参见文献[4](图2)。
1.2.2 制定手术计划 在规划单元的屏幕上显示经直肠前列腺超声的轴状面, 调整手件使手件的纵轴与经直肠超声探头平行, 确保手件与水平线对齐。在超声显像的前列腺轮廓上规划切除的深度与范围(图3A), 即高压水柱扫除的角度和扇面。对于不对称增生的前列腺侧叶, 其切除的范围和深度也是不对称的; 对于中叶突入膀胱明显的患者, 可调节超声探头显示前列腺中叶并单独设置。调整超声显像至矢状面, 显示前列腺全部轮廓, 在显像上设定标注切除起始位置、膀胱颈、前列腺前部、前列腺中部、结束位置等, 顺滑连接各标记, 即形成需要切除的前列腺轮廓(图3B), 注意突入膀胱内的中叶应被包括在内而尿道括约肌需被排除在外。
1.2.3 高压水束切除 按压手件上的“ +” 按钮确认手术计划, 踩下踏板开始进行水刀切除, 将高压、高速生理盐水柱从手件上喷嘴喷出, 并按照控制台设置的程序进行操作, 手件可进行左右旋转和前后移动。利用水刀的切割功能, 切除前列腺组织, 切下的组织随水流带入膀胱(图3C)。为维持膀胱容量平衡, AquaBeam系统带有负压抽吸功能, 可通过手件抽吸膀胱内的液体和组织, 利用蠕动泵控制速度。对于大体积前列腺, 在切除完毕后可根据残存前列腺大小, 选择再次制定计划, 进行切除[5]。
1.2.4 止血 切除结束后, 解锁关节臂, 移除AquaBeam系统, 应用双极电凝对创面进行电凝止血, 术中出血部位主要在膀胱颈部。电切镜下见创面表面不光滑, 出血不多, 表面无焦灼, 未发现穿孔或静脉窦开放部位, 冲洗液清亮后留置三腔尿管, 持续牵拉6 h后解除压迫, 持续冲洗至冲洗液清亮。也可以直接放置三腔尿管持续牵拉压迫止血[4]。
例1手术时长65 min(设备安装时间30min, 术前规划15min, 水刀消融时间2 min14 s, 检查止血10min), 术中估计出血量约20 mL; 例2手术时长45 min(设备安装时间20min, 术前规划10min, 水刀消融时间3 min28 s, 检查止血10min), 术中估计出血量约30 mL。
例1持续冲洗19 h后, 冲洗液清亮, 停止冲洗3 d后拔除尿管出院。例2持续牵拉5 h后, 出现膀胱痉挛, 冲洗液颜色由淡红转为鲜红, 进而变为深红, 并出现膀胱填塞。于术后8 h急诊行膀胱凝血块清除、双极电凝止血术, 术中自膀胱内清除凝血块约400 mL, 但创面未发现明确的动脉出血, 术后输注3 u红细胞。术后第4天冲洗液清亮, 停止膀胱冲洗, 术后1周拔除尿管并出院。
术后病理2例患者均为前列腺增生, 均在术后1个月内发生过2次轻微肉眼血尿, 未经特殊处理, 1 d后自行消失, 未出现尿潴留、尿失禁、泌尿系感染及严重LUTS症状。随访3个月, 例1的IPSS为11分, 较术前下降16分(59.3%); QOL为2分, 较术前下降3分(60%); 经直肠超声测量前列腺体积为29.3 mL, 较术前减少22.1 mL(43%); Qmax术后17.9 mL/s, 较术前上升11.8 mL/s(增加193.4%); 剩余尿量(post void residual, PVR)19 mL, 减少47 mL(71.2%)。例2术后IPSS为5分, 较术前下降15分(75%); QOL为3分, 较术前下降1分(25%); tPSA 1.43 μ g/L, 较术前下降2.84 μ g/L, 恢复到正常值; 经直肠超声测量前列腺体积为23.9 mL, 减少29.7 mL(55.4%); Qmax9.1 mL/s, 上升5.9 mL/s(增加184.4%); PVR为144 mL, 减少54 mL(27.3%)(表1)。
| 表1 术后随访3个月时的专科情况 |
水刀消融是一种新型的治疗BPH的手术方法。该技术利用水刀的高速水流切割作用, 使用机器人控制水流, 进行实时成像引导的半自主组织消融。其设计原理是, 外科医生在经直肠超声监视下, 精确地绘制移行区和切除靶区, 使用高压水流在电脑控制下, 提供一个一致的、可量化的和标准化的无热治疗, 优先切除腺体组织, 保留胶原结构, 如外科包膜、膀胱颈和血管[6]。其优势是高效、无热切除, 并能最大限度地减少外科医生间的差异[7]。
该技术最早在2015年被使用于临床[8], 越来越多的文献支持水刀消融术能改善BPH患者的LUTS症状, 保护患者的性功能。Gilling等[9]在一项多中心随机双盲对照研究中比较了机器人水刀消融术和经典TURP的疗效和安全性, 在6个月的随访时, 两组患者在IPSS评分的改善(P=0.14)、QOL评分改善(P=0.47)、Qmax(P=0.1)、PVR(P=NS)等均无显著差别, 但在较大体积前列腺(50~80 mL)的分层分析中, 水刀消融组IPSS评分的改善显著优于TURP组(P=0.02); 总体的不良事件发生率低于TURP组(25.9%vs. 41.5%, P< 0.02), 勃起功能障碍或射精功能障碍的发生率低于TURP组(6.9% vs. 24.6%, P< 0.01), Clavien-Dindo 2级以上不良事件的发生率两组相当(19.8% vs. 23.1%, P=NS), 水刀消融组略优。Misrai等[4]在一项多中心注册研究中, 由3名无操作经验的外科医生执行该项技术, 在症状改善、并发症的发生率、性功能的保留方面获得了类似的结果。Desai等[5]的研究也证明水刀消融术对大体积前列腺(80~150 mL)患者安全、有效, 是一种可接受的手术选择。在一项多中心的前瞻性研究中, 178名患者中56例患者出现了69例不良事件。其中Clavien-Dindo 1级事件33例, 2级事件15例, 3a级事件5例, 3b级事件16例, 术后1周内, 14例(7.9%)患者行二次手术止血; 5例(2.8%)患者接受了输血[10]。出血是机器人水刀消融术最常见的严重并发症, 早期采用激光或电凝止血, 近年的研究中多报道采用三腔尿管持续牵拉压迫, 而出血的不良事件发生率并无显著提高, 也没有因为患者前列腺体积的增加而增高[11]。
目前, 经尿道前列腺机器人水刀切除系统已经成为唯一通过美国FDA、欧盟CE的泌尿外科专用手术机器人, 并纳入相应的诊疗指南[12, 13]。但相关研究、手术数据在国内未见报道。本研究率先在国内开展2例机器人水刀前列腺消融术并介绍其经验, 患者的纳入、排除标准如前所述, 手术方案的设计与实施同时结合国外最新研究及既往经尿道前列腺手术的经验。研究详细记录2名接受前列腺水刀消融术患者的病程及随访资料, 手术均顺利完成, 水刀消融时间极短, 仅分别为2 min14 s、3 min28 s, 出血也较少, 术中估计出血量分别约20 mL、30 mL。例1术后4 d出院。例2在围手术期发生了Clavien-Dindo 3a级的并发症, 予以急诊膀胱凝血块清除、双极电凝止血术, 我们认为主要原因是牵拉导致的膀胱痉挛引发了膀胱颈部出血, 形成了膀胱填塞。术后随访3个月2例患者均无尿潴留、尿失禁、泌尿系感染及严重的LUTS症状。2例患者术后IPSS、QOL均较术前降低, 术后前列腺体积明显减小, Qmax较术前增加, 例1术后PVR较术前明显减少, 但例2术后PVR仍有144 mL, 考虑患者由于膀胱填塞导致膀胱功能下降, 术后尿动力学检查显示患者最大尿流率时逼尿肌压力为3.136 kPa(32 cmH2O), 较术前有所下降[下降0.98 kPa(10 cmH2O)), 也支持此观点。本文结果与国外多中心研究结果相近, 但仅为个例, 旨在介绍此项技术在我中心初次开展的经验, 后续将继续开展临床研究, 期于确定国内机器人前列腺水刀切除的临床数据。
新世纪以来, 随着能量技术的引进, BPH的外科治疗经历了重大革新, 目前经尿道前列腺剜除术(transurethral enucleation of prostate, TUEP)、HoLEP和PVP在临床被广泛应用。但这些技术的手术时间较机器人水刀消融技术均较长, 且随前列腺体积的增加延长明显, 而水刀消融技术的手术时间增加并不显著。而且TUEP和HoLEP技术要求高, 学习曲线陡峭, 且术后短暂性尿失禁的发生率较高[14, 15, 16, 17, 18]; 而PVP技术虽然临床输血率低, 但手术时间较长, 且随前列腺体积的增加明显增加。当然, 这些结论仅来自文献的荟萃对比, 尚需要机器人水刀消融术与这些技术的直接对照研究来证明。
综上所述, 现有的国外研究证明, 机器人水刀消融技术安全、有效, 且具有高效、性功能影响小、稳定、对医生技术要求低等特点, 是可选择的一项治疗BPH的新型外科治疗技术, 本中心目前详细描述该手术流程, 同时小样本研究结果与国外研究结果相佐, 但仍需要纳入更多样本数据, 期于寻找更适合国内机器人前列腺水刀切除的纳入排除标准, 和手术、术后治疗、随访程序。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|