尿石症是一种极为常见的疾病, 自从出现体外冲击波碎石术(extracorporeal shock wave lithotripsy, ESWL), 输尿管镜碎石术(ureteroscopic lithotripsy, URL)和经皮肾镜取石术(percutaneous nephrolithotomy, PCNL)以来, 输尿管结石的治疗手段已发生了重大变化, 后腹腔镜输尿管切开取石术(retroperitoneal laparoscopic ureterectomy, RLUL)通常被认为是治疗最复杂结石的终极手段, 并且始终占据着重要的位置[1]。我们在临床中已经认识到RLUL在某些患者中的潜力和优势, 尤其对于一些合并严重感染的患者, RLUL可以作为最佳选择, 并且可以在有效清石的基础上确保患者安全康复[2]。对于输尿管上段结石合并同侧肾结石的患者, 如何在保证安全的前提下有效清石, 仅通过一期手术, 同时取净同侧的肾、输尿管结石值得研究, 我们在临床中发现通过RLUL+胆道镜(choledochoscopy, COC)碎石取石, 解决了这一问题, 具有临床实用价值和应用前景, 值得推广[3]。
回顾分析2018年2月– 2020年4月在我院接受RLUL+COC和PCNL治疗的输尿管上段结石合并同侧肾结石患者的临床资料, 分别有48例和46例纳入研究。患者的病史、临床表现及泌尿系彩超、腹部平片、泌尿系CT、IVU等检查结果符合纳入标准。纳入标准:①输尿管上段结石合并同侧肾结石, 同时合并中、重度积水; ②输尿管结石长径> 1.5 cm, 单发, 结石位于第4腰椎横突水平以上; ③肾脏结石位于肾盂或肾盏, 非鹿角形结石。排除标准:①合并严重高血压、脑血管意外及心脏病和肝肾功能不全、凝血功能障碍等疾病; ②治疗依从性差, 无法完成随访; ③存在其他手术禁忌证。尿白细胞阳性患者给予抗感染治疗, 复查转阴后手术, 其中尿培养阳性患者选择敏感抗生素治疗1周以上。高血压、糖尿病患者控制血压、血糖在正常水平。本研究经我院伦理委员会审批通过, 入组患者均签署知情同意书。
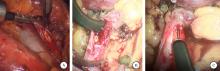
RLUL+COC组实施RLUL+COC碎石取石。患者接受全身麻醉, 术前留置尿管。取健侧卧位, 常规三孔法建立后腹腔。清理腹膜外脂肪, 打开肾周筋膜, 分离出肾后间隙, 在腰大肌、肾下极与腹膜之间的三角区域内游离出输尿管。找到输尿管结石所在位置, 在结石上方用无损伤抓钳夹住输尿管, 以防结石上移至肾脏。有触石感时, 在结石上端根据结石大小切开合适的长度, 将结石取出(图1A)。然后将胆道镜从切口置入(图1B), 肾内小结石采用套石网篮取出, 若结石长径较大则先采用钬激光碎块化模式碎石, 而后采用套石网篮取出(图1C)。将F6双J管沿斑马导丝置入, 4-0可吸收线缝合输尿管切口, 取出结石, 彻底止血, 留置引流管, 缝合皮肤切口。术后3 d行KUB平片或泌尿系CT检查, 术后引流量持续3 d少于10 mL时拔除引流管及导尿管, 留置双J管4~6周。
PCNL组采取PCNL。患者接受全身麻醉, 膀胱截石位经尿道逆行留置输尿管导管及导尿管, 然后改俯卧位, 腰腹垫高。选取患侧肾中上盏后组盏作为穿刺点建立人工肾积水, B超引导下穿刺目标盏穹隆部, 穿刺针芯见尿液滴出后证实穿刺成功, 留置斑马导丝, 使用F8~F18筋膜扩张器逐级扩张, 留置F18剥皮鞘, 建立皮肾通道。置入F8.5 Wolf输尿管镜, 检查各肾盏、肾盂、输尿管上段, 寻及结石后使用钬激光或气压弹道碎石, 击碎结石从通道冲出, 清石后留置F5双J管及肾造瘘管。术后5 d行肾造瘘管造影检查, 若集合系统通畅, 无明显残余结石, 拔除肾造瘘管及导尿管, 留置双J管4~6周。
1.3.1 围手术期观察指标 围手术期观察指标包括:手术时间、术中出血量及术后住院时间、Ⅰ 期结石清除率、并发症发生率。术中出血量计算方法[4]:将引流液混匀, 抽取5 mL用血红蛋白检测仪检测血红蛋白浓度, 出血量(mL)=引流液中血红蛋白浓度(g/L)× 引流液的量(L)/术前血红蛋白浓度× 1 000。Ⅰ 期清石率(stone-free rate, SFR)[5]:术后复查KUB片或CT平扫(针对阴性结石或平片未能清晰显示者), 以影像学检查提示结石排净或残石≤ 2 mm定义为清石成功, SFR(%)=A/(A+B)100%, A为术后影像学提示结石排净或残石≤ 2 mm的病例数, B为术后影像学提示残石> 2 mm的病例数。
1.3.2 术后随访 术后3个月复查B超或泌尿系CT, 扩张肾盂减小程度≥ 1.0 cm表示肾积水缓解。术后患者均获得有效随访, 随访时间6~24个月, 定期行泌尿系彩超等检查, 观察有无输尿管狭窄及结石复发。
采用SPSS 18.0软件包处理数据。患者的一般资料、手术时间、术中出血量及术后住院时间等计量资料比较采用t检验, 结石清除率及并发症发生率等计数资料比较采用χ 2检验, P< 0.05为差异有统计学意义。
RLUL+COC组48例患者手术过程顺利, 无中转开放病例。手术时间为(70.25+11.34)min, 术中出血量(50.36± 26.84)mL, 术后住院(5.46± 2.02)d, 术后复查Ⅰ 期SFR为95.83%(46/48)。2例术后出现尿脓毒血症等感染相关并发症, 加强抗感染后治愈; 2例手术后出现漏尿, 复查KUB发现双J管下移, 重新调整双J管位置后治愈。术中、术后未发生大出血、肠道损伤等并发症, 复查泌尿系彩超显示肾积水患者积水消失或明显改善。随访患者未出现输尿管狭窄。
PCNL组43例一期完成手术, 3例分期手术(2例因术中出血, 1例因穿刺为脓尿)。手术时间为(92.54± 20.27)min, 术中出血(110.66± 32.62)mL, 术后住院(7.58± 3.18)d, 术后复查Ⅰ 期SFR为82.61%(38/46)。术后4例出现尿脓毒血症, 经加强抗感染后治愈; 术后4例患者出现明显出血, 其中3例保守治疗成功, 1例行介入栓塞后治愈。复查泌尿系彩超显示肾积水患者积水消失或明显改善。随访患者未出现输尿管狭窄。
RLUL+COC组手术时间、术中出血量、住院天数均低于PCNL组(P< 0.05); RLUL+COC组的Ⅰ 期结石清除率(95.83%)与PCNL组(82.61%)相比, 差异有统计学意义; RLUL+COC组并发症发生率(8.33%)低于PCNL组(17.39%), 差异有统计学意义(见表2)。
| 表2 两组术中、术后观察指标比较 $\bar{x}$± s |
ESWL、URL、PCNL等治疗手段在临床广泛应用, 但仍存在一定的局限性。如果结石质地较硬、体积偏大合并解剖学异常等因素, 则ESWL清石率低[6]; URL处理输尿管上段结石时常因结石上移需二期手术或需辅助ESWL再治疗; 对于输尿管上段结石合并肾结石, PCNL兼顾处理有一定难度, 单通道时碎石角度不佳容易造成盏颈撕裂, 多通道时又增加肾实质损伤和出血的风险[7]。对于结石负荷较大、质硬、局部息肉包裹、合并肾盂输尿管解剖异常需同期处理的输尿管上段结石, RLUL因具有损伤小、出血少、恢复快等优点, 具有一定优势[8, 9, 10]。
我们在临床工作中发现, 有很多输尿管上段结石合并肾结石的病例, 后腹腔镜对于处理输尿管上段结石安全、有效, 但处理肾结石, 尤其是肾盏结石时往往较难。我们在前期研究中发现, 因输尿管上段结石近端输尿管扩张, 结石有上移至肾脏的情况, 我们尝试从输尿管切口置入胆道镜, 结合套石篮取出上移的结石, 效果很好。于是我们决定将二者结合起来, 采用“ 双镜联合” 处理输尿管上段结石合并肾结石的病例[11]。由于胆道镜镜体柔软光滑, 容易通过扭曲的输尿管, 对输尿管、肾盂黏膜损伤小, 镜体末端可上下弯曲, 可以观察和处理肾盂、肾盏结石, 弥补了后腹腔镜对肾结石清除不够彻底的问题[12]。患者接受后腹腔镜联合胆道镜治疗肾、输尿管结石, 疗效满意。
在我们的实践中, 由于术者已经具备了腹腔镜及软镜的基础, 所以将两者联合运用时, 难度并不大, 学习曲线不长。主要有以下原因:①胆道镜可直接由穿刺套管直接置入, 不用重新建立通道; ②胆道镜镜体柔软光滑, 容易通过输尿管扭曲或狭窄处; ③双镜联合时与常规软镜的操作没有区别, 肾内结石只需碎块化处理, 加以套石网篮取出, 清石效率明显提高。在实际工作中, 初学者在运用双镜联合时需要具备空间三维立体感, 还要注意胆道镜从输尿管切口进入和上行过程中, 用力轻柔, 不要对输尿管过多的牵扯, 避免不必要的损伤。术中寻找输尿管需要一定的经验和技巧:在腰大肌、肾脏下极、腹膜之间的三角区往往能较快游离出输尿管。取石后留置输尿管双J管往往成为初学者的难题, 我们使用吸引器套管作为支撑, 沿斑马导丝留置输尿管双J管取得了满意效果; 输尿管切口的缝合有一定难度, 在后腹腔狭小的空间内缝合打结需要术者具备一定的腔镜缝合技术。
本研究中我们应用后腹腔镜联合胆道镜治疗输尿管上段结石合并肾结石有以下优点:①处理输尿管结石的同时处理肾结石, 在微创条件下可一期完成手术, 减轻了患者的痛苦, 降低了患者的经济负担; ②胆道镜操作时可以经输尿管切口引流灌注液, 保持集合系统低压状态, 减少了因灌注压高引发的感染; ③经输尿管切口处理肾结石, 不需建立皮肾通道, 不破坏肾脏实质, 对肾功能影响小, 同时降低了肾脏损伤及出血的风险; ④胆道镜自输尿管上段切口进入输尿管并逆行直达肾盂、肾盏, 进镜路径短, 而且由于近端输尿管扩张, 胆道镜上行难度小, 无须前期留置双J管; ⑤与输尿管软镜相比, 胆道镜镜体较短, 操作方便, 而且工作通道更大, 在置入550 μ m钬激光光纤或套石直径更大的网篮后, 仍然可以保持视野清晰, 增加了碎石效率, 减少了手术时间[13]。
与RLUL+COC相比, PCNL需要建立皮肾通道, 破坏了肾实质, 增加了肾脏损伤和出血的风险; PCNL术中肾盂压力高, 术后出现泌尿系感染的风险较大; PCNL在术中需要变换体位, 手术环节相对比较复杂; 而且PCNL需要采取俯卧位, 会对患者的心、肺造成压迫, 因而对患者的心、肺功能要求较高[14]。而RLUL+COC不存在以上问题。此外, RLUL+COC在解剖学上还有一定优势:由于在腹膜后空间进行操作, 对腹腔内脏器干扰小, 不影响肠道功能, 减少了肠道损伤和术后肠梗阻的发生, 同时也能够降低术后尿液渗漏引起腹腔感染以及远期并发症的发生率[15]。
我们的研究结果发现与PCNL相比, RLUL+COC组的手术时间、术中出血量、住院天数均低于PCNL组, 结石清除率高于PCNL组, 并发症发生率低于PCNL组, 说明后腹腔镜联合胆道镜治疗输尿管上段结石合并肾结石具有创伤小、术后恢复快、结石清除率高、并发症少的优点, 在临床上有很好的应用前景, 对于肾结石负荷不大, 同时合并感染的病例, 该术式是很好的选择[16]。而对于鹿角形结石等负荷过大的结石, 有学者证实双镜联合的治疗依然安全有效[17, 18]。
作为单个中心的回顾性研究, 我们的研究也有其局限性。尽管RLUL+COC可以提供令人满意的结果, 但是手术过程相对复杂限制了其在临床的广泛应用。此外, 我们随访的时间比较短, 缺乏远期的观察结果。我们下一步准备对RLUL+COC展开进一步研究, 扩大观察的样本量, 延长随访时间, 获得更可靠的数据, 同时使手术方式标准化, 从而有利于推广。
本研究结果表明, RLUL联合使用胆道镜治疗输尿管上段结石及肾结石具有安全、高效、创伤小、术后恢复快等优点, 是复杂上尿路结石微创治疗的选择途径之一。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|