目的: 探讨机器人辅助腹腔镜完全腹膜外化异体肾移植术可行性。方法: 2019年1–3月完成机器人辅助完全腹膜外化异体肾移植术3例。移植肾经脐部切口至于髂外血管内侧,依次完成动静脉及膀胱输尿管吻合,后将移植肾翻转至于右侧髂窝,位于腹膜外,缝合原覆盖在髂外血管上的腹膜,实现肾脏腹膜外化。结果: 3例患者顺利完成手术,手术耗时138~189 min(除外机器人系统准备时间),供肾热缺血时间50 s~1 min,术后第7天血肌酐99.3~122.2 μmol/L。术后随访1个月均无并发症发生。结论: 完全腹膜外化机器人辅助肾移植安全、可行,可以应用于终末期肾病患者。
Objective: To investigate the feasibility of robotic-assisted kidney transplantation in complete peritoneal externalization to treat end-stage renal disease.Methods: Three patients received robotic-assisted kidney transplantation during January to March, 2019. The transplanted kidney was transfused through the umbilical incision to the medial side of the external iliac vessels, followed by arteriovenous and cystoureteral anastomoses. The transplanted kidney was turned over to the right iliac fossa, outside the peritoneum. The peritoneum covering the external iliac blood vessels was sutured to achieve the peritoneum externalization of the kidney.Results: Three patients underwent the operation successfully. Operation time was 138-189 min (except docking time of robot system). The warm ischemia time was between 50 s and 1 min. The serum creatinine was 99.3-122.2 µmol/L at the 7th day postoperatively. All patients were followed up for 1 month without postoperative complications.Conclusions: The robotic-assisted kidney transplantation with complete peritoneal externalization is safe and feasible. It can be used to treat end-stage renal disease.
肾移植是终末期肾病的最佳治疗方法, 虽然传统的开放肾移植手术(open kidney transplant, OKT)仍然是金标准[1], 但随着达芬奇手术系统(Da Vinci surgical system, dVSS)的发展, 机器人肾移植手术(robotic-assisted kidney transplant, RAKT)逐渐受到人们的青睐。机器人手术需要更大的操作空间, 首次报道RAKT技术的Giulianotti等[2]将移植肾放在腹腔内, 2011年Boggi等[3]改进了手术方式, 首次报道机器人辅助腹腔镜完全腹膜外化肾移植术, 目前, 国外仅有少数移植中心成功开展了此项手术。2019年1– 3月我院泌尿外科成功完成了3例完全腹膜外化RAKT, 现报告如下。
3例患者均为男性, 年龄28~49岁。BMI 18.9~20.83 kg/m2。术前血肌酐911.0~1 008.3 μ mol/L, 尿素氮13.78~19.93 noml/L, 均诊断为慢性肾功能不全(尿毒症期)。2例供肾者为患者母亲, 1例供肾者为患者姐姐, 均系自愿无偿捐献。供肾者既往体健, 术前检查无肾脏捐献禁忌证或手术禁忌证。
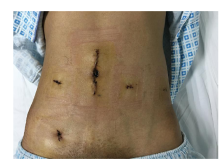
常规后腹腔镜切取供肾, 切口位置(图1A)、气腹建立及Trocar位置摆放(图1B)均参照文献[4]进行。
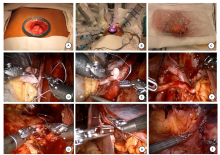 | 图1 手术方法 A:腹部中央切口; B:Trocar位置; C:自制冰袋; D:肾静脉与髂外静脉端侧吻合; E:肾动脉与髂外动脉端侧吻合; F:肾脏放置于右侧髂窝; G:膀胱输尿管吻合; H:关闭原覆盖在髂外血管上的腹膜, 实现肾脏腹膜外化; I:腹膜外化完成。 |
充分游离耻骨后膀胱前壁, 扩大手术视野并为膀胱输尿管吻合做准备。沿髂外血管纵行切开覆盖在其上的腹膜约8 cm, 充分游离髂外血管及右侧髂窝, 同时保护好打开的腹膜, 为移植肾完全腹膜外化做好准备。将供肾(左肾)置入自制塑料肾袋并填塞冰屑(图1C), 在肾门处开口。将移植肾从脐部切口置入腹腔, 放置在髂外血管内侧, 使肾动静脉朝向髂外血管, 输尿管朝向膀胱。重新建立气腹, 用血管阻断夹阻断右髂外静脉, 纵行剪开1.5 cm开口, 采用6/0 Gore-Tex CV-6缝合线将供肾静脉与右髂外静脉行端侧吻合(图1D)。完成静脉吻合之前, 可经辅助孔用F5输尿管导管在静脉内注入肝素盐水冲洗管腔。吻合完成后用血管夹阻断肾静脉, 打开髂外静脉的血管夹, 检查无明显出血。以相同方式行肾动脉和髂外动脉端侧吻合(图1E), 血管夹阻断肾动脉, 打开髂外动脉的血管夹, 检查无明显出血。依次开放肾静脉、肾动脉, 观察肾脏再灌注情况及输尿管口尿液流出情况, 将肾脏翻转后置入右侧髂窝, 位于腹膜外(图1F)。纵行切开膀胱右侧顶壁肌层约2.5 cm, 用5-0 Monocryl缝合线将供肾输尿管与膀胱外黏膜下吻合(图1G), 间断缝合膀胱肌层, 输尿管内留置双J管。关闭原覆盖在髂外血管上的腹膜, 实现肾脏腹膜外化(图1H、图1I)。
3例患者顺利完成手术, 手术耗时138~189 min(除外机器人系统准备时间), 供肾热缺血时间50 s~1 min, 冷缺血时间82~199 min, 动脉吻合时间17~22 min, 静脉吻合时间19~26 min, 输尿管吻合时间23~33 min, 术后第7天血肌酐值99.3~122.2 μ mol/L, 术后7~11 d出院(图2)。术后随访1个月均无并发症发生。
随着腔镜技术及机器人手术系统的发展, 微创肾移植术再次成为人们关注的焦点, 其中, 机器人手术系统凭借其高清放大3D视野、可弯曲机械臂及减震滤颤的效果、可提高重建手术管腔吻合的精度及速度等优势[5], 为RAKT的发展提供了极佳的技术平台。传统OKT多经Gibson切口, 采用腹膜外入路完成血管吻合及尿道重建, 将移植肾置于腹膜外。而机器人手术系统则需要更大的操作空间[5, 6], 因此RAKT多经腹操作, 将移植肾置于腹腔内。Giulianotti等[2]首次报道RAKT技术, 也选择将15例患者的移植肾放在腹腔内, 但将移植物置于腹腔内有其明显的局限性, 主要表现为①肾扭转风险:位于腹腔内的移植肾活动度大, 易发生肾扭转而导致移植肾损坏。Modi等[7]的报告中72例病例中, 有1例出现肾扭转; ②术后肾穿刺活检损伤大[8]:腹腔内的移植肾术后多经腹腔镜肾活检, 相比于腹膜外化的移植肾, 更容易出现肠损伤及活检后腹腔出血的问题; ③出血及尿瘘是术后常见的并发症:腹腔引流管拔出后若发生延迟性出血或尿瘘, 因腹腔容量过大而不易被察觉, 易导致诊断治疗延误。总之, 移植肾腹膜外化更加符合人的生理结构, 同时也避免了移植肾位于腹腔内的局限性[9, 10]。
目前国内外学者正积极探索肾脏腹膜外化方法。Boggi等[3]用宽幅绷带将患者固定在手术台上, 将手术床向左倾斜至Trendelenburg's体位, 通过耻骨上Pfannenstiel切口放入肾脏并进行血管吻合, 最后将移植肾置于腹膜外。Menon等[11]及Breda等[12]采用经典的前列腺癌根治术体位, 通过在绕脐切口放置GelPOINT来完成放入肾脏和维持气腹, 并事先切开盲肠旁腹膜制成一个腹膜瓣, 最后将移植肾缝合于腹膜瓣中, 实现肾脏的腹膜外化。还有一些学者采用了完全腹膜外操作技术, 从而使肾脏在手术全程均位于腹膜外。Tsai等[13]让机器人手臂抬高腹壁3 cm来为操作提供空间, 通过Gibson切口放入肾脏进行血管吻合。Bruyè re等[14]通过Alexis切口完成腹膜外入路RAKT。Michiels等[15]在不切开腹膜的前提下, 制作了一个脐周6 cm的切口, 用手指不断扩大腹膜外间隙的操作空间直到找到髂血管, 完成了完全腹膜外的RAKT。Raveendran等[16]及Adiyat等[17]则通过脐下的Pfannenstiel切口来完成手术, 其中Adiyat等报道了世界范围内最多的完全腹膜外操作移植手术的病例。但完全腹膜外操作是一个难度相当高的手术, 尤其对于肥胖患者, 手术空间更小, 操作难度更高[13, 15, 17], 要求术者兼备丰富的机器人及肾移植手术经验, 手术方式尚需优化和完善以达到过程标准化, 且各术式的远期疗效缺乏长期的随访结果, 不建议在技术尚不成熟时盲目开展完全腹膜外肾移植手术。
本研究腹膜外化的方法与Menon等[11]学者的类似, 并参考其他研究[3]做出了改进:游离髂外动静脉时保护好原先覆盖在血管上的腹膜, 先把肾脏放置在髂外血管内侧的腹膜内完成血管吻合, 后将肾脏翻转放入右侧腹膜下的髂窝内, 待完成膀胱输尿管吻合后, 缝合覆盖在髂血管上的腹膜, 完成腹膜外化。这种方式无需事先切开盲肠旁腹膜制作腹膜瓣, 节省手术时间, 减少肾脏的冷缺血时间, 利于肾脏的功能恢复。
当然, 肾脏腹膜外化也存在潜在的缺点和限制。有报道曾提到会增加淋巴囊肿的可能性[17], 但国内外已报道的文献中未见出现。由于腹膜关闭后无法看到肾脏, 使关腹前无法再次检查肾脏周围有无漏血、漏尿。另外, 当供体的肾脏过大且受者本身又较为瘦小时, 由于受者右侧髂窝空间较小, 强行的腹膜外化可能会导致过大的肾脏血供或者回流不畅, 存在肾脏压迫肾动静脉以及髂内外动静脉的风险。
综上, 完全腹膜外化RAKT安全、可行, 摆脱了移植肾位于腹腔内的固有局限, 更加符合人体生理结构, 可以应用于终末期肾病患者。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|